TP 5 : le volume
molaire, réaction entre l’acide chlorhydrique et le métal magnésium
I) mis en évidence des
espèces présentes dans l’acide chlorhydrique
1) dans un tube à essais
verser 1 mL de solution d’acide chlorhydrique, ajouter quelques gouttes de
nitrate d’argent (Ag+,NO3-).
Q1 : qu’observe-t-on ?
Q2 : quelle espèce met-on
en évidence ? Ecrire l’équation bilan de la réaction de précipitation.
2) déposer une goutte d’acide
chlorhydrique sur un petit morceau de papier indicateur de pH.
Q3 quel est le pH ? Quel
ion est mis en évidence ?
Q4 : donner la formule de
la solution d’acide chlorhydrique.
II) Réaction entre le métal
magnésium et l’acide chlorhydrique
1) aspect qualitatif
a) identification des
produits formés
introduire dans un tube à
essais 1 ou 2 mL d’acide chlorhydrique et un petit morceau de magnésium (5 mm
de ruban)
Q5 : qu’observe-t-on ?
Le professeur mettra en évidence le gaz qui se dégage.
Q6 : verser quelques
gouttes d’hydroxyde de sodium (Na+ , HO-). Qu’observe-t-on ?
Quel ion est mis en évidence ? Ecrire la réaction de précipitation qui c’est
produite.
b) Equation bilan de la
réaction
Q7 : identifier les
espèces chimiques présentes dans le système initial et dans le système final. Ecrire
l’équation chimique de la réaction.
III) détermination du
volume molaire Vm des gaz
1) expérience
Peser la masse m d’une
longueur L =30 cm d’un ruban de magnésium
Q8 : en déduire la masse linéique
du ruban
Réaliser le montage suivant :
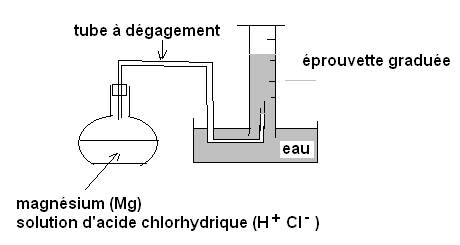
Calculer la masse de m de 3 cm de ruban. A l’aide d’une éprouvette
graduée introduire dans un ballon un volume Va = mL d’acide chlorhydrique de concentration
Ca = mol.L-1, puis la masse m
connue de magnésium.
Q9 : à la fin de la
réaction, relever le volume V (H2) de dihydrogène qui c’est dégagé.
2) calcul du volume molaire
Q10 : Calculer la
quantité de matière de magnésium (Mg) introduite dans le ballon (M(Mg) =
24g.mol.g-1. Sachant que le magnésium est le réactif en défaut en
déduire la quantité de matière de dihydrogène n(H2) qui c’est dégagé.
Q11 Calculer le volume molaire
Vm.