Suivi spectrophotométrique
d'une réaction
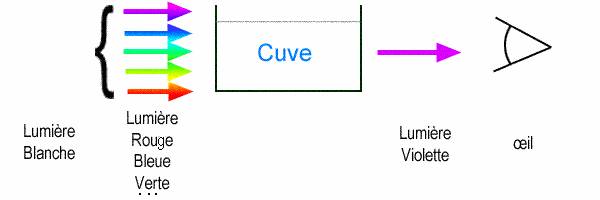
a) L'espèce concernée par la mesure est l'ion permanganate. Il donne une
coloration violette à la solution, qui absorbe une partie du rayonnement
incident.
b) Pierre a raison, Marie pouffe, mais elle ferait mieux d'arrêter les chamalos, et se mettre au travail.
k = 2,25 x 103
L.mol-1
Q2
a) L'espèce concernée par la mesure est toujours l'ion permanganate MnO4-,
les autres espèces étant incolores.
b) L'absorbance A = k.C . Or A diminue, donc la
concentration C, en ion permanganate, diminue.
c) La demi-réaction d'oxydation correspondant à l'acide oxalique est :
H2C2O4
= 2CO2 + 2H+ + 2e-
Pour voir un exemple comment équilibrer une équation d'oxydoréduction, clique
ici. Cette réaction correspond à une perte d'électrons, c'est une réaction
d'oxydation donc l'acide oxalique H2C2O4
est l'espèce réductrice ( elle fournit gracieusement les électrons ).
Q3
a) La vitesse volumique v(t) d'une réaction calculée à l'instant t, est
égale à la dérivée de l'avancement "x" par rapport au temps, divisée
par le volume "V" de solution :
![]()
b) Réponse partielle, pour voir la vidéo, clique
ici.
V = V1 + V2 + V3 = 2.5 x 10-3
L
Tableau d'avancement en mol.L-1
:
|
État du système |
Avancement
(mol) |
2
MnO4- (mol.L-1) |
5 H2C2O4
(mol.L-1) |
2Mn2+
(mol.L-1) |
|
État Initial |
x =0 |
0.8x10-3 |
2x10-3 |
0 |
|
En cours |
x |
0.8x10-3 - 2x/V |
2x10-3 - 5x/V |
2x/V |
|
État final |
xmax |
0 |
0 |
0.8x10-3 |
c) Réponse partielle, pour voir la vidéo clique
ici.
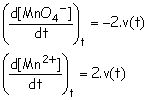
Q4
a) Réponse partielle, pour voir la vidéo, clique
ici.
![]()
b) Pour voir la réponse vidéo, clique
ici.
c) Comment évolue la vitesse 'v' au cours du temps ?
pour 100 < t < 230 , X augmente, donc la vitesse 'v' augmente également
pour t > 230
, X diminue, donc la vitesse
'v' aussi.
a) Le rôle d'un catalyseur est d'augmenter la vitesse de la réaction,
sans intervenir dans son équation bilan.
b) Le catalyseur permet d'accélérer la réaction, mais au fur et à mesure
que l'avancement 'x' de la réaction augmente, la concentration en réactifs
diminue, entraînant une décroissance de la vitesse de réaction.