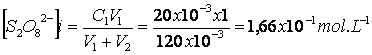Réaction entre les ions peroxodisulfate et iodure
1)
Concentration initiale des ions peroxodisulfate dans
le mélange réactionnel.
2)
La réaction fournit du diiode(I2)
et des ions sulfate (SO42-). Ecrire
l’équation qui se déroule entre les deux réactifs.
½
réaction de réduction (gain d’électrons)
S2O82-
+2e- =
2SO42-
½
réaction d’oxydation (perte d’électrons)
2I- = I2 + 2e-
équation
d’oxydoréduction
S2O82-
+ 2 I- = 2 SO42- + I2
3)
Vidéo
La
réaction se termine quand il n’y a plus d’ions S2O82-
n1
– xmax = 0
C1V1
– xmax = 0
xmax = 20x10-3 mol
ou
quand il n’y a plus d’ions I-
n2
– 2xmax = 0 ; xmax =
n2/2 = C2V2/2 = 5x10-2 mol
5x10-2 mol >
20x10-3 mol , le réactif en excès est l’ion
iodure, le mélange n’est pas stœchiométrique
4)
Vidéo
Les
valeurs des quantités de matière sont en mole
|
Etat du
système |
Avancement |
S2O82- |
2 I- |
2 SO42- |
I2 |
|
État initial |
x = 0 |
C1V1 = 2x10-2 |
C2V2=
10-1 |
0 |
0 |
|
En cours |
x(t) |
2x10-2-x(t) |
|
2x(t) |
x(t) |
|
Etat final |
x = xmax =2x10-2 |
0 |
10-1-2xmax=
6x10-2 |
2xmax
= 4x10-2 |
xmax = 2x10-2 |
5)
a) Déterminer la relation entre la valeur de l’avancement au cours
du temps x(t) et n(S2O82-)
t
n(S2O82-)
t = 2x10-2-x(t)
x(t)
= 2x10-2 - n(S2O82-)
t
b)
Tracer la courbe x(t)
|
t(min) |
0 |
2.5 |
5 |
10 |
15 |
20 |
25 |
30 |
|
n(S2O82-)
x10-3 mol |
20 |
18 |
16.6 |
14.1 |
12.3 |
10.8 |
9.6 |
8.8 |
|
x(t)
= 2x10-2-n(S2O82-)
t |
0 |
2 |
3.4 |
6.9 |
7.7 |
9.2 |
10.4 |
11.2 |
6)
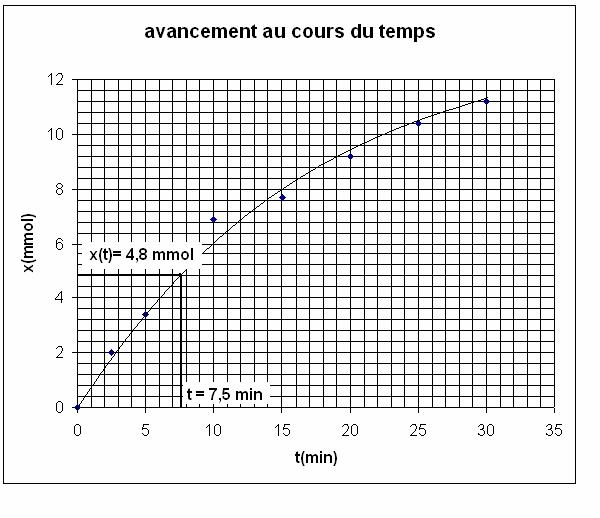
Déduire de la courbe à t =
7,5 minutes la quantité de matière de diiode
formée.
D’après
la courbe ci dessus à t = 7,5 min :
x(7,5
min) = 4,8x10-3 mol
or
d’après le tableau d’avancement x(t) = n(I2)formé,t
donc
n(I2)formé, t =
7,5 min = 4,8x10-3
mol