A propos de l’acide formique (USA Bac 2004) énoncé
Q1
a) Calcul de
la masse m d’acide formique.
Co
= 0,01 mol.L-1 ; Vo = 100 mL = 0,1 L; M(HCOOH) = 2.M(H) +
M(C) + 2.M(O) = 2 + 12 + 2x16 = 46 g.mol-1
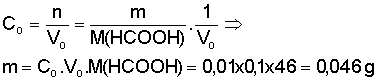
Pour préparer la solution, il
faut utiliser 0,046 g d’acide formique.
b) Réaction acido-basique
entre l’acide formique et l’eau :
HCOOH aq + H2O(l)
= HCOO-aq + H3O+aq
Pour les
étourdi(e)s : n’oubliez pas d’indiquer dans quel état se trouvent les
espèces chimiques (aqueuse pour les ions).