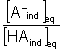Chapitre 5 : constante d’acidité d’un couple acide base
Les indicateurs colorés naturels de la cuisine à la chimie.
1.1 Suivant le pH de la solution, l’indicateur coloré change de teinte.
1.2 Le vinaigre a des propriétés acide car au contact de l’indicateur coloré la solution se colore en rouge.
Le détergent a des propriétés basiques car au contact de l’indicateur coloré la solution devient verte.
2.1 Prendre une pipette jaugée de 20 mL et une fiole jaugée de 200 mL (verrerie précise)
K
La quantité de matière de vinaigre prélevée dans la solution mère (concentration Cm) est égale à la quantité de matière de vinaigre se trouvant dans la solution fille (concentration Cf ):
nm = nf Þ
![]()
La solution mère est diluée 10 fois.
2.2.1 Vidéo
Equation de
dosage
CH3-CO2H
aq + Na+aq
+ HO-aq = CH3-CO2-
aq + H2O(l) + Na+aq
2.2.2 Vidéo
VB < VE le réactif limitant est le réactif titrant (l’hydroxyde de sodium)
2.2.3
VB = 6,0 mL ; la quantité de matière de soude versée est : nB = CB.VB
Si la réaction de dosage est totale (le réactif limitant étant la soude):
CBVB – xmax = 0 Þ
xmax = CB.VB = 10-1 x 6 x 10-3 = 6 x 10-4 mol
2.2.4 Vidéo
D’après la courbe pour VB = 6 mL, pH = 5
Or [H3O+]
= 10-pH et [H3O+].[HO-] = Ke Þ
![]()
n(HO-)f = [HO-].(VA+VB+Veau) = 10-9 x 76 x 10-3 = 7,6 x 10-11 mol
2.2.5 taux d’avancement final
CBVB – xf = n(HO-)f Þ xf = CBVB – n(HO-)f = 6 x 10-4 – 7,6 x 10-11 » 6 x 10-4 mol = xmax
![]()
La réaction de dosage est totale.
2.3.1 A l’équivalence, la valeur de (dpH/Vb) est maximale.
Graphiquement VBE = 10 mL
2.3.2 A l’équivalence les réactifs sont introduits dans les proportions stoechiométriques :
cAVA = cB.VBE
![]()
2.4.1 Vidéo
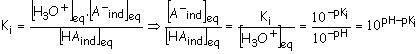
2.4.2 et 2.4.3
Exemple de calcul pour la betterave avec un pH = 6,5
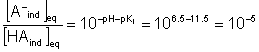
|
|
Artichaud |
Betterave |
||
|
|
VB = 9.8 mL |
VB = 10,1 mL |
VB = 9.8 mL |
VB = 10,1 mL |
|
|
-1 |
3 |
-5 |
-1 |
|
couleur |
incolore |
jaune |
Rouge |
Rouge |
2.4.4 le meilleur indicateur coloré est l’artiche car le pH à l’équivalence est compris dans sa zone de virage.
2.4.5 Un vinaigre coloré gène par sa couleur le dosage colorimétrique.