Ibuprofène
Q1
a) D'après les données, l'ibuprofène a une grande solubilité dans
l'éthanol, et une très faible solubilité dans l'eau.
L'ibuprofène contenu dans le cachet va se solubiliser dans l'éthanol, et
grâce à la filtration, on pourra le séparer de l'excipient du médicament (celui
ci est insoluble dans l'éthanol !).
b) Couple acide base: RCOOH/RCOO- ; H2O/HO-
RCOOHaq + Na+aq + HO-aq
= RCOO-aq + H2O + Na+aq
Q2
Tout d'abord, le sage écrit toujours les données, les convertit dans la
bonne unité, et recopie l'équation bilan du dosage acido-basique. Il peut alors
se concentrer sur les beautés de ce monde….
RCOOHaq + Na+aq + HO-aq
= RCOO-aq + H2O + Na+aq
Mibu = 206 g.mol-1 ; mibu = 0,2 g par
gélule; Cb = 9 x 10-3mol.L-1 ; Vb = 0,2 L;
On compare ensuite le nombre de moles de base initiale divisé par son
coefficient stœchiométrique (1), avec le nombre de moles d'ibuprofène
initial, divisé par son coefficient stœchiométrique (1).
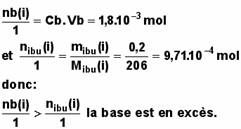
L’autre méthode consiste à déterminer l’avancement maximal
pour les 2 réactifs. L’avancement maximal le plus petit correspond au
réactif en défaut.
Q3
Réponse partielle, pour voir la vidéo clique
ici.
a) H30+ + Cl- +
Na+ + HO- = 2 H2O + Na+ + Cl-
b) nb(excès) = 8,6 x 10-5 mol
c) K = 1014
Q4
Réponse partielle, pour voir la vidéo clique
ici.
m (ibu) = 0,194 g ;
Pourcentage d'erreur relative : 3 %
Q5
a) Question très souvent posée, pour vérifier que vous connaissez bien la
verrerie et autres appareils utilisés!
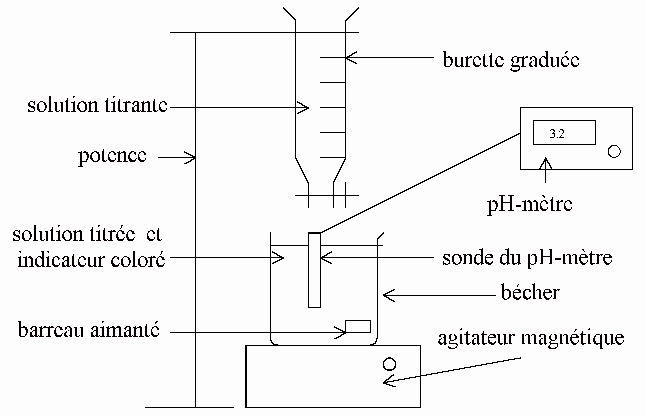
La solution titrante est l'acide chlorhydrique (H3O+,Cl-),
la solution titrée, l'hydroxyde de sodium (Na+,HO- )
b) L'indicateur colorée est le bleu de bromothymol. En effet il va changer de
teinte à l'équivalence, puisque sa zone de virage est comprise entre pH=6 et pH
= 7,6 et qu'elle contient le point équivalent de la courbe de dosage. Lorsque la solution change de teinte l'expérimentateur sait qu'il se
trouve approximativement à l'équivalence: le nombre de mole d'acide versé est
égal au nombre de mole de base présent dans le bécher.