Chapitre 4 :
LES SPECTRES LUMINEUX
La spectroscopie est
l'étude et l'interprétation des spectres de rayonnements.
A - SPECTRES D'EMISSION
1-
DEFINITION :
Un
spectre d’émission est un spectre produit par la lumière directement émise
par une source (lampe à incandescence, corps chauffé, lampe à vapeur de
sodium…)
2– SPECTRE CONTINU
D’EMISSION DE
On réalise le montage de
décomposition de la lumière par un prisme et on fait varier la tension et donc
la puissance reçue par la lampe. Noter vos observations et conclure : On observe un spectre continu d’émission qui s’enrichit en
radiations violettes quand la température augmente.
Fortement
chauffé, un corps émet un rayonnement d’origine thermique dont le spectre
est continu. L’allure du spectre dépend de la température du corps. Plus la
température est élevée, plus le rayonnement s’enrichit en radiations de
courtes longueurs d’onde cad violet. Le spectre
se prolonge au-delà du spectre visible, dans le domaine de l’infrarouge et
de l’ultraviolet.
3- SPECTRE DE RAIES
D'EMISSION :
On analyse la lumière
émise par différentes lampes spectrales à l'aide d'un prisme à vision directe.

3.1.
Lampe à vapeur de Mercure :
On observe
plusieurs raies discontinues cad séparées de noire : 1 raie jaune-orangée, 1 raie verte, 1 raie indigo et 1 raie violette.
3.2. Lampe à vapeur de Cadnium :
On observe plusieurs raies discontinues : 1 raie rouge, 1 raie verte, 1 raie turquoise et 1 raie bleue.
3.3. Lampe à vapeur de :
On observe
une seule raie jaune.
4- CONCLUSIONS :
Les
gaz portés à haute température émettent une lumière dont le spectre est
discontinu : c’est un spectre de raies d’émission, constitué de raies
colorées sur fond noir.
B - SPECTRES D’ABSORPTION
1-
DEFINITION :
Un spectre d’absorption est obtenu en analysant la
lumière blanche qui a traversé une substance.
2-
SPECTRE DE RAIES D'ABSORPTION D’UN
GAZ : LE SODIUM
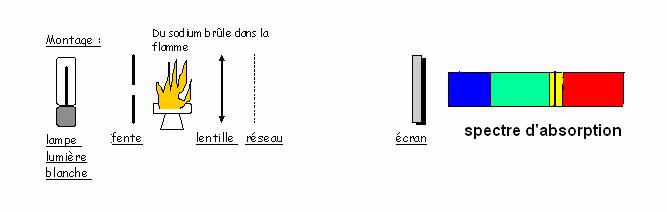
- Quel est le spectre observé avant de
placer le sodium en combustion ? spectre continu
-
Quelle modification observe-t-on lorsque
l'on interpose la flamme jaune du sodium dans le faisceau de lumière blanche ? raie noire dans la partie jaune du spectre continu
-
Comparer avec le spectre d'émission du
sodium. Conclure.
Lorsqu’un
gaz à basse température est traversé par de la lumière blanche, le spectre
de la lumière obtenue est constitué de raies noires se détachant sur le
fond coloré du spectre de la lumière blanche : c’est un spectre de
raies d’absorption. Le gaz absorbe les radiations qu’il serait capable
d’émettre s’il était chaud. Pour un même élément, les raies d’émission
(dans le spectre d’émission) et d’absorption (dans le spectre d’absorption)
ont les mêmes longueurs d’onde.
3-
SPECTRE DE BANDES D'ABSORPTION D’UNE SOLUTION COLOREE :
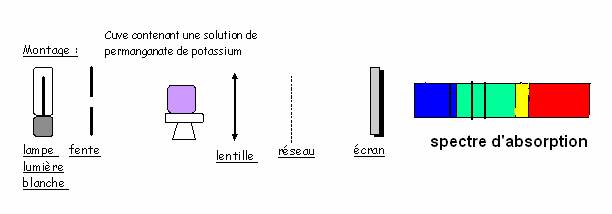
- Quel est le spectre observé avant de
placer la cuve ? spectre continu
-
Quelle modification observe-t-on lorsque
l'on interpose la cuve dans le faisceau de lumière blanche? Bande noire dans la partie bleue-verte du spectre continu
-
Reprendre l'expérience avec une solution de
sulfate de cuivre ou de bichromate de potassium. Conclure. Bande noire dans la partie rouge et bande noire dans la
partie bleue-violette
Lorsqu’une
solution colorée est traversée par de la lumière blanche, le spectre de la
lumière obtenue présente des bandes noires sur le fond coloré du spectre de
la lumière blanche : c’est un spectre de bandes d’absorption. Ce
spectre est caractéristique de la substance dissoute.n