Chapitre 10 :
estérification-hydrolyse
2003
Pondichéry I. Étude d'une
estérification (6 points)
Données
:
·
pKA (CH3COOH
/ CH3COO–) = 4,8 ; pKe = 14 .
·
Masses
atomiques molaires: H =
·
Masse
volumique du propan-1-ol :
On étudie la cinétique de la formation d'un ester à partir d'acide éthanoïque et de propan-1-ol.
On
maintient, à la température constante q, sept erlenmeyers
numérotés 1, 2 ,3...7, contenant chacun un mélange de 0,500 mol d'acide
éthanoïque et de 0,500 mol de propan-1-ol.
Ces erlenmeyers sont tous préparés à l'instant t = 0 et on dose d'heure en heure l'acide restant dans le mélange. On peut ainsi en déduire la quantité de matière d'ester formé:
à t = 1 h , dosage de
l’erlenmeyer n°1,
à t = 2 h ,
dosage de l’erlenmeyer n°2 , etc.
1) La réaction d'estérification
a)
En
utilisant les formules semi-développées, écrire l'équation de la réaction
d'estérification et nommer l'ester formé.
b)
On dispose
d'un flacon de propan-1-ol pur. Quel volume de cet alcool doit-on verser dans
chacun des sept erlenmeyers ?
c) Exprimer la quantité de matière d'ester formé dans un erlenmeyer à une date t en fonction de la quantité de matière d'acide restant.
2) Titrage de l'acide restant :
Mode opératoire :
A
la date t considérée, le contenu de l'erlenmeyer est
versé dans une fiole jaugée puis dilué avec de l'eau distillée pour obtenir 100
mL de solution. On en prélève 5 mL
que l'on verse dans un bécher. On titre cette solution par une solution
d'hydroxyde de sodium de concentration cb = 1,0 mol.L-1.
On en déduit la quantité de matière d'acide restant dans le bécher puis dans
les 100 mL de départ, ce qui permet de déterminer la
quantité d'ester au temps t dans les 100 mL de
départ.
a)
Écrire
l'équation chimique de la réaction de titrage.
b)
Rappeler
la définition de la constante d'acidité de l'acide éthanoïque. En déduire l'expression de la constante
d'équilibre K associée à la réaction de titrage. Calculer la valeur numérique de K. Cette réaction de titrage
peut-elle être considérée comme totale ?
c)
Pour l'erlenmeyer n°l (t = l h), le volume de
solution de soude versé pour atteindre l'équivalence est de 14,2 mL. En déduire
la quantité de matière d'acide restant dans l'erlenmeyer
et la quantité de matière d'ester formé.
3) Cinétique de la réaction d'estérification:
Le
titrage des solutions contenues dans les sept erlenmeyers
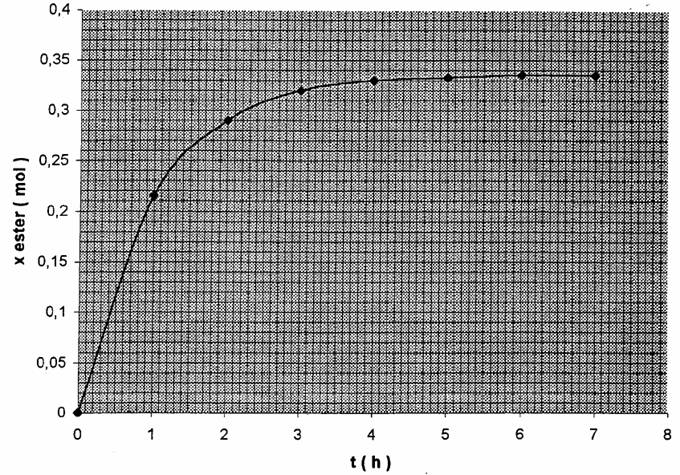
précédents a permis le tracé de la courbe donnée en annexe
a) Dresser le tableau descriptif de l'évolution du système. Déterminer l'avancement maximal xmax ainsi que l'avancement à l'équilibre xeq .Comparer ces deux valeurs et déterminer le rendement r de la réaction.
b) Rappeler l'expression de la vitesse volumique v d'une réaction. Quelle interprétation géométrique ou graphique peut-on en donner ? Comment cette vitesse évolue-t-elle au cours de la transformation ? Justifier.
c) Calculer la constante d'équilibre K' de cette réaction d'estérification.
d) Pour déplacer l'équilibre, on ajoute une mole d'acide supplémentaire. Calculer le quotient de réaction Qr et déterminer le sens de l'évolution du système.
Déterminer les nouvelles valeurs de l'avancement à l'équilibre et du rendement de la réaction.
ANNEXE 1
( Cinétique de la réaction d'estérification).
x ester = f(t)