Chapitre 10 : estérification-hydrolyse
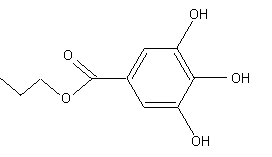
De la poudre de tara au gallate de propyle (Liban 2005)
Le gallate de propyle, de masse molaire
Il est utilisé comme
additif alimentaire pour ses propriétés anti-oxydantes, il est identifié par le
code E310.
Le gallate de propyle peut être obtenu à partir de
l'acide gallique dont les caractéristiques sont données ci-dessous :
L'acide gallique :
Nomenclature : Acide
3,4,5-trihydroxybenzoïque
Formule semi-développée :
C6H2(OH)3-COOH
Formule topologique :
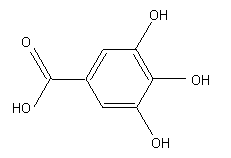
Masse molaire : M =
Solide à la température ambiante; température de fusIon
Solubilité: très peu soluble dans l'eau froide, soluble
dans l'eau chaude
Couple acide gallique / ion gallate : pKa = 3,1
L'acide gallique est extrait du tanin contenu dans
les gousses des fruits du tara, arbuste du Pérou.
A – « Extraction » de l'acide gallique
Le tanin est extrait de
la poudre de tara par dissolution dans l'eau chaude et filtration. On
additionne de l'hydroxyde de sodium solide NaOH(s) au filtrat pour
obtenir un pH de l'ordre de 11. On chauffe à reflux pendant une trentaine de
minutes en présence de pierre ponce. La saponification du tanin produit l'ion
gallate. Après refroidissement dans la glace, on ajoute de l'acide
chlorhydrique concentré, le pH de la solution atteint la valeur 1,5 et l'acide
gallique précipite .
1.
a) Compléter la légende du
schéma du montage de chauffage à reflux porté en annexe à joindre à la
copie.
b)
Indiquer l'intérêt du
chauffage à reflux.
c)
Comment peut-on rapidement
s'assurer que le pH atteint la valeur souhaitée ?
2.
Écrire la formule
semi-développée de l'ion gallate.
3.
Dans cette question on notera
AH l'acide gallique et A– l'ion gallate.
a)
Écrire l'équation modélisant
la réaction de l'acide gallique avec l'eau.
b)
Donner l'expression de la
constante d'acidité Ka du couple AH/A–
c)
Calculer le rapport des
concentrations à l'équilibre [AH]eq I [A- ]eq
dans la solution de pH égal à 1,5. (On acceptera le résultat numérique sous
forme de puissance de dix non entière).Indiquer l'espèce prédominante.
d) Représenter sur un axe de pH les domaines de prédominance de AH et A–
. Justifier.
e)
Pourquoi refroidit-on le
mélange réactionnel ?
f)
Indiquer un procédé permettant de vérifier la
pureté de l'acide gallique.
B – De l'acide gallique au galIate de propyle
On réalise un mélange équimolaire d'acide gallique
et d'un alcool B. Après addition d'acide sulfurique concentré, le mélange est
chauffé à reflux pendant une heure. On obtient ainsi le gallate de propyle.
1.
Nommer le groupe
caractéristique obtenu, et l'entourer dans la formule topologique du gallate de
propyle reproduite en annexe.
2.
Donner la formule
semi-développée et le nom de l'alcool utilisé pour cette synthèse.
3.
a) Écrire l'équation de la réaction de synthèse du
gallate de propyle.
b) Nommer cette réaction. Indiquer deux caractéristiques principales de
cette réaction.
c) Quel est le rôle de l'acide sulfurique ?
d) Quel est le rôle de la pierre ponce ?
4.
Le rendement de la synthèse
est de 70%.
Quelle
masse de gallate de propyle peut-on espérer obtenir à partir d'une masse m =
5.
Pour préparer le gallate de
propyle a-t-on intérêt à utiliser de l'alcool en excès ?Justifier.
EXERCICE I : ANNEXE A RENDRE AVEC
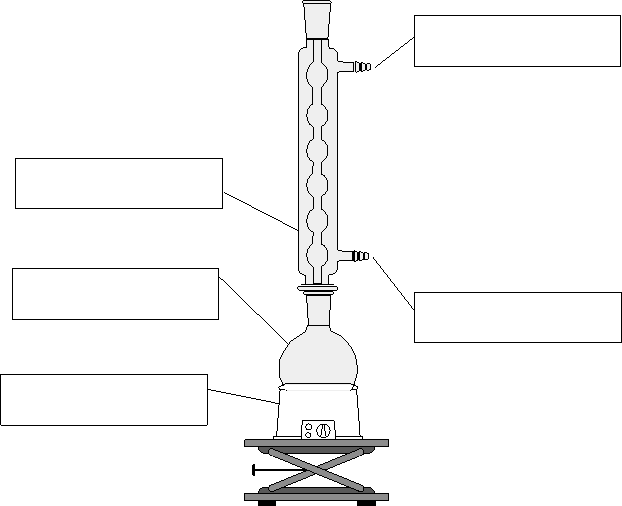
Le montage de chauffage à reflux
Formule topologique du gallate de propyle: