Chapitre 11 : contrôle de l'évolution d'un système
Bizarre, bizarre... ( métropole Bac 2004)
Il y a quelques décennies, les femmes lavaient le linge au lavoir en utilisant un mélange de suif (graisses animales) et de cendres. On cherche à comprendre ici comment ces deux produits salissants permettent le nettoyage.
Q1
La cendre.
a) Les cendres étaient recueillies dans un pot et mélangées à de l'eau. La cendre de bois contient de la potasse KOH. Sachant que la potasse contient des ions potassium K+ , écrire l'équation traduisant la réaction associée à la dissolution de la potasse solide dans l'eau.
b) Le suif. Le suif est composé majoritairement de tristéarate de glycéryle dont la formule est :
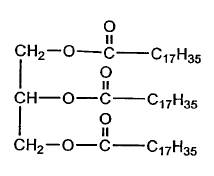
À quelle famille chimique appartient le tristéarate de glycéryle ? Recopier la formule et entourer les groupes caractéristiques (ou fonctionnels) correspondant à cette famille.
c) Donner la formule de l'acide (sans le nommer), ainsi que la formule et le nom de l'alcool nécessaire pour fabriquer le tristéarate de glycéryle. Comment se nomme cette réaction ?
Q2
Le mélange de suif et de cendres...
a) En utilisant les formules semi-développées, écrire l'équation chimique de la réaction modélisant la transformation lors du mélange de suif et de cendres.
b) Par cette réaction, on obtient un savon qui a des propriétés nettoyantes. Ce produit possède une partie hydrophile et une partie lipophile. Identifier la partie hydrophile de l'ion négatif contenu dans ce savon et préciser la définition du terme hydrophile.