Polynésie septembre 2005 Calculatrice autorisée
EXERCICE II : FERMENTATION DANS LE
VIN (6,5 points)
« Le vin est une boisson provenant exclusivement de la
fermentation du raisin frais ou du jus de raisin frais ».
Telle est la définition
légale du vin mais derrière le terme « fermentation » se cachent des
transformations que les chimistes ont mis des années à découvrir.
Dans les années 1960, on commença à s'intéresser à une autre
fermentation qui se produit généralement après la fermentation alcoolique et à
laquelle on n'attachait pas trop d'importance jusqu'alors car on pensait qu'il
s'agissait d'un achèvement de la fermentation alcoolique.
Il s'agit de la fermentation malolactique qui consiste en une
transformation totale de l'acide malique présent dans le jus de raisin en acide
lactique sous l'action de bactéries.
Cette fermentation, longtemps ignorée, a une influence reconnue sur la
qualité gustative de certains vins à condition de la conduire convenablement. .
Les techniques actuelles de suivi de ces fermentations se font par
dosage enzymatique ; elles consistent essentiellement à doser l'alcool contenu dans
le vin.
Principe du dosage :
Étape 1 : On effectue une
distillation du vin de telle façon que l'on recueille une solution incolore
contenant tout l'éthanol présent dans le vin.
Étape 2: L'éthanol est oxydé par la
nicotinamide-adénine-dinucléotide (NAD+) dans une réaction catalysée
par une enzyme spécifique. La réaction produit de la
nicotinamide-adénine-dinucléotide réduite (NADH) en quantité de matière égale à
celle de l'éthanol dosé selon l'équation :
CH3CH2OH + NAD+ = CH3CHO +
NADH + H+ (1).
Étape 3 : On mesure l'absorbance de
la NADH par spectrophotométrie à la longueur d'onde de 340 nm lors du dosage.
A – Premiere partie: Determination
du degre alcoolique d'un vin
« On appelle
degré alcoolique d'une boisson alcoolisée, le volume (exprimé en mL) d'éthanol contenu dans
100 mL de cette boisson, les volumes étant mesurés à 20°C. »
On
l'exprime en % vol.
I - Questions préliminaires
1. Montrer que la réaction (1)
est bien une réaction d'oxydo-réduction en faisant
apparaître le transfert d'électrons entre les deux couples donnés.
Couples
d'oxydo-réduction: CH3CHO / CH3CH2OH NAD+ / NADH
2. Quel est le rôle du
catalyseur ?
Il
- Étalonnage du spectrophotomètre
On
réalise une gamme de quatre solutions étalons; chaque solution étalon contient
:
- NAD+ en excès,
- Le catalyseur,
- Une solution de concentration massique connue en éthanol.
On
mesure l'absorbance de chaque solution étalon et on obtient les résultats suivants
:
|
Solution étalon |
S1 |
S2 |
S3 |
S4 |
|
Concentration massique Cm en éthanol en mg.L-1 |
50 |
100 |
200 |
300 |
|
Absorbance : A |
0,08 |
0,16 |
0,32 |
0,48 |
1.
Lors du réglage initial, quelle valeur doit-on donner à l'absorbance de la
solution de référence avant toute mesure ?
2.
Tracer la courbe A en fonction de la concentration massique.
3.
Montrer que la représentation graphique est en accord avec la loi de
Beer-Lambert A = kCm.
Déterminer la valeur de k en L.mg–1.
III - Préparation et dosage de l'éthanol
contenu dans le vin
On distille 20
mL de vin ; le distillat est ensuite ajusté à 200 mL avec de l'eau distillée
pour obtenir une solution appelée D.
On prépare l'échantillon à doser par spectrophotométrie en introduisant
:
-
1
mL de solution D,
-
Le
catalyseur,
-
NAD+
en excès,
dans une fiole jaugée de 50
mL que l'on complète avec de l'eau distillée.
L'absorbance mesurée pour cet échantillon vaut: Ae = 0,30.
1.
Montrer que l'échantillon préparé correspond à une dilution au 1/50e
de la solution D.
2.
Par une méthode de votre choix à préciser, déterminer à partir de
l'absorbance mesurée Ae la concentration massique en éthanol de
l'échantillon étudié.
3.
En déduire la concentration massique en éthanol :
a)
de la solution D.
b)
du vin.
4.
Déterminer alors le degré alcoolique du vin.
Donnée: - Masse volumique de
l'éthanol supposée constante dans le domaine de concentration
considéré: 0,80 kg.L-1
B – Deuxieme partie: cinetique de la fermentation
malolactique
L'équation de la fermentation malolactique est :
COOH-CH2-CHOH-COOH = CH3-CHOH-COOH
+ CO2
Acide malique Acide lactique
Le dosage enzymatique de l'acide
malique restant dans le vin a donné les résultats suivants pour une température
de fermentation maintenue à 20°C
|
Concentration
massique Cm(t) en acide malique (g.L-1) |
3,5 |
2,3 |
1,6 |
0,8 |
0,5 |
0,27 |
0 |
|
Date
t (en jours) |
0 |
4 |
8 |
12 |
16 |
20 |
28 |
1.
Montrer que la concentration molaire en acide malique restant dans le vin à
l'instant t s'exprime par: [acide malique] (t) = ![]() .
.
En déduire la quantité de matière d'acide malique n acide malique
(t = 0) initiale dans un litre de vin.
2. A
l'aide d'un tableau descriptif de l'évolution de la réaction, montrer que
l'avancement à l'instant t de cette réaction pour un litre de vin se met sous
la forme :
x(t) = 2,6 x 10–2 – n acide malique (t)
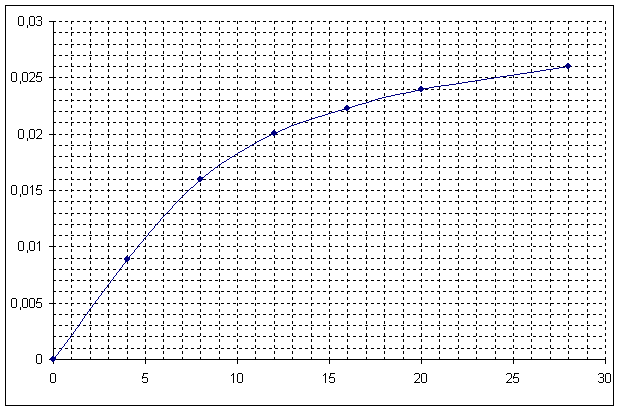
3. La courbe représentant les variations de x en fonction du
temps t est donnée en annexe.
a) Calculer la vitesse volumique à l’instant t =0.
b) Commenter l'évolution de la vitesse volumique de la
réaction au cours du temps.
4. Définir et déterminer le temps de demi réaction.
Données: MC = 12 g.mol-1; MO = 16 g.mol-1 ; MH = 1,0 g.mol-1
Annexe: Fermentation dans
le vin x = f(t)
Évolution de l'avancement en fonction du temps
x en mol
t en jours![]()
![]()