Chapitre
5 : constante d’acidité d’un couple acide base
Les
indicateurs colorés naturels de la cuisine à la chimie (métropole bac national
6,5 points)
La première utilisation d'un indicateur coloré pour les titrages
acido-basiques remonte à 1767 par
W. Lewis. Il employait
un extrait de tournesol (...) .On utilisait à l'époque des extraits de plantes
qui changent de couleur avec l'acidité du milieu (...). On peut en citer
quelques-uns parmi les plus connus et les meilleurs :
- l'artichaut (...)
- la betterave rouge (...)
- le chou rouge, de loin l'extrait le plus
intéressant car sa couleur change nettement suivant la valeur du pH :
pH 0-3 4-6 7-8 9-12 13-14
couleur rouge
violet bleu vert jaune
d'après Chimie des couleurs et des odeurs
1.
Des
indicateurs colorés en cuisine.
Le chou rouge est un légume riche en fibres et en vitamines, qui se
consomme aussi bien en salade que cuit. Mais la cuisson du chou rouge peut
réserver des surprises: chou rouge et eau de cuisson deviennent rapidement
bleus. Pour rendre au chou sa couleur violette, on peut ajouter un filet de
citron ou du vinaigre. Après avoir égoutté le chou, une autre modification de
couleur peut surprendre le cuisinier: versée dans un évier contenant un détergent,
l'eau de cuisson devient verte. En
utilisant les textes ci-dessus
1.1.
Donner
la propriété essentielle d'un indicateur coloré acido basique.
1.2.
Préciser
le caractère acide ou basique du vinaigre et du détergent.
2.
Des
indicateurs colorés pour les titrages.
De nos jours, les indicateurs colorés sont toujours largement utilisés
pour les titrages. La pH-métrie est une autre technique de titrage
acido-basique qui permet en outre de choisir convenablement un indicateur
coloré acido-basique pour ces mêmes titrages. Dans la suite de l'exercice, on
s'intéresse au titrage de l'acide éthanoïque de formule CH3 – CO2H
(noté par la suite HA) contenu dans un vinaigre commercial incolore. La base
conjuguée de cet acide sera notée A– .
2.1.
Dilution
du vinaigre.
Le vinaigre commercial étant trop concentré pour être titré par la
solution d'hydroxyde de sodium disponible au laboratoire, on le dilue dix fois.
On dispose pour cela de la verrerie suivante :
Éprouvettes : 5 mL 10 mL 25
mL 50 mL 100 mL
Pipettes
jaugées : 1,0 mL 5,0 mL 10,0 mL 20,0
mL
Fioles jaugées : 150,0 mL 200,0 mL 250,0
mL 500,0 mL
Choisir dans cette
liste la verrerie la plus appropriée pour effectuer la dilution. Justifier.
2.2.
Réaction
de titrage.
On titre un volume VA = 10,0 mL de la solution diluée de
vinaigre par une solution aqueuse
d'hydroxyde de sodium (ou soude) de concentration molaire en soluté
apporté cB = 1,0 ´ 10–1 mol.L-1.
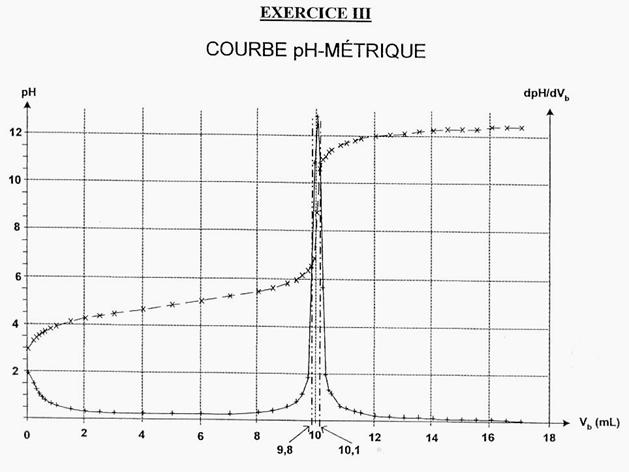
On ajoute un volume Veau = 60 mL afin d'immerger les électrodes du pH-mètre après agitation.Le suivi pH-métrique de la transformation permet de construire la courbe fournie dans l'ANNEXE À RENDRE A VEC LA COPIE. Cette partie a pour but de vérifier que la transformation associée à la réaction de titrage est totale. Pour cela, on déterminera son taux d'avancement final pour un volume VB = 6,0 mL de solution aqueuse d'hydroxyde de sodium versé. Donnée :produit ionique de l'eau à 25°C Ke = 10 –14
2.2.1.
Écrire l’équation
associée à la réaction de titrage.
2.2.2.
Pour VB
= 6,0 mL, déterminer le réactif limitant.
2.2.3.
Pour VB
= 6,0 mL, déterminer l'avancement maximal xmax . On pourra s'aider d'un tableau d'avancement.
2.2.4.
Après
avoir relevé la valeur du pH du mélange obtenu, déterminer la quantité de
matière d'ions hydroxyde restante après la transformation (n![]() )f dans le volume total de mélange réactionnel.
)f dans le volume total de mélange réactionnel.
2.2.5.
Déterminer
le taux d'avancement final et conclure.
2.3.
Détermination
par titrage de la concentration molaire en acide éthanoïque apporté du
vinaigre.
2.3.1.
Déterminer
graphiquement sur l'ANNEXE À RENDRE AVEC LA COPIE le volume de la
solution d'hydroxyde de sodium versé à l'équivalence. Préciser la démarche
utilisée.
2.3.2.
Déterminer
la valeur de la concentration molaire en acide éthanoïque apporté cA
dans le vinaigre dilué et en déduire la valeur de la concentration molaire en
acide éthanoïque apporté c0 du vinaigre commercial.
2.4. Retour historique …On souhaite réaliser un titrage colorimétrique de l'acide éthanoïque
contenu dans le vinaigre dilué
avec un des deux extraits naturels (artichaut et betterave rouge)
utilisés au dix huitième siècle. Pour chaque indicateur coloré, on considère
que les teintes sont dues à la prédominance d'une espèce chimique, notée HAInd
pour sa forme acide et A–Ind pour sa forme basique. Le pKa des couples HAInd/ A–Ind
sera noté pKi.
On donne les valeurs des pKi à 25°C :
artichaut: (pKi )1 = 7,5
betterave rouge: (pKi)2
= 11,5
|
|
Artichaut |
Betterave |
|
pKi |
7,5 |
11,5 |
|
Teinte pour HAInd dominant |
incolore |
rouge |
|
Teinte pour A–Ind dominant |
jaune |
jaune |
2.4.1.
En utilisant
l'expression de la constante d'acidité Ki,
montrer que la relation suivante est vérifiée :
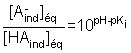
On s'interroge sur les couleurs que prendrait le mélange réactionnel lors
du titrage colorimétrique de l'acide éthanoïque en présence d'une petite
quantité de l'un ou l'autre de ces extraits naturels.
2.4.2. La courbe
pH-métrique montre que, pour VB = 9,8 mL, le pH de la solution est
voisin de 6,5 et que, pour VB
= 10,1 mL, il est voisin de 10,5.
Pour chaque
extrait naturel et pour chacun de ces deux volumes VB, déterminer la
valeur du rapport :
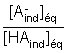
puis compléter
la ligne correspondante du tableau de l'ANNEXE À RENDRE AVEC LA COPIE.
2.4.3. En déduire les couleurs observées dans chaque
cas. Compléter la ligne correspondante du tableau de l'ANNEXE À RENDRE AVEC
LA COPIE.
2.4.4.
Conclure
sur l'indicateur coloré le plus adapté pour ce titrage.
2.4.5.
Pourquoi
faut-il choisir un vinaigre incolore pour ce type de titrage ?
TABLEAU
|
|
Artichaut |
Betterave |
||
|
|
VB = 9,8 mL |
VB = 10,1 mL |
VB = 9,8 mL |
VB = 10,1 mL |
|
|
|
|
|
|
|
Couleur |
|
|
|
|