Chapitre 5 : constante d’acidité
d’un couple acide base
A propos de l’acide formique ( Bac
USA 2004)
Q1
Pour se défendre, les
fourmis utilisent deux moyens : leurs mandibules et la production d’acide
formique. Les mandibules servent a immobiliser l’ennemi tandis que l’acide
formique brûle la victime. Une fourmi se sentant menacée se dresse sur ses deux pattes arrière et peut projeter
sur l’ennemi un jet d’acide formique à plus de 30 cm grâce à son abdomen.
L’acide formique (ou acide méthanoïque) soluble dans l’eau a pour formule
semi-développée HCOOH. On se propose d’étudier quelques propriétés d’une
solution aqueuse de cet acide.
Données :
- Masses molaires
atomiques : M (C) = 12 g.mol-1 ;
M (H) = 1 g.mol-1
; M(O) = 16 g.mol-1
- Constante d’acidité à
25 °C :
KA (HCOOH/HCOO-)
= 1,8 x 10-4
- Conductivité molaire
ionique à 25 °C (conditions de l’expérience) : l(H3O+) = 35,0 x 10-3
S.m2.mol-1 ;
l(HCOO-) = 5,46 x 10-3 S.m2.mol-1.
On rappelle l’expression
de la conductivité s d’une solution en
fonction des concentrations molaires des espèces ioniques Xi
dissoutes :
![]()
a) Dans une fiole jaugée
de volume Vo = 100 mL, on introduit une masse m d’acide formique
puis on complète cette fiole avec de l’eau distillée jusqu’au trait de jauge
puis on homogénéise. On dispose alors d’une solution d’acide formique de
concentration molaire Co = 0,01 mol.L-1 ; Calculer
sa masse m
b) Ecrire l’équation de
la réaction associée à la transformation de l’acide formique en présence d’eau.
Q2
a) Etablir un
tableau d’avancement correspondant à cette transformation chimique, en fonction
de Co, Vo, xmax et xeq. On note xeq
l’avancement à l’état d’équilibre et xmax l’avancement de la
réaction supposée totale.
b) Exprimer le taux
d’avancement final t en fonction de la
concentration en ions oxonium à l’équilibre [H3O+]eq
et de Co.
c) Donner
l’expression du quotient de réaction à l’état d’équilibre Qr,eq.
Montrer que ce quotient peut s’écrire sous la forme :
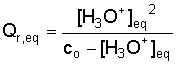
Q3
a) Exprimer la
conductivité de la solution d’acide formique à l’état d’équilibre en fonction
des conductivités molaires ioniques des ions présents et de la concentration en
ions oxonium à l’équilibre [H3O+]eq.
b) La mesure de la
conductivité de la solution So donne s = 0,05 S.m-1 à 25 °C. En utilisant les relations obtenues
précédemment compléter le tableau ci-dessous.
|
Solution |
So |
S1 |
|
Ci(mol.L-1) |
0,010 |
0,10 |
|
s(S.m-1) |
0,050 |
0,17 |
|
[H3O+]eq
(mol.m-3) |
|
4,2 |
|
[H3O+]eq
(mol.L-1) |
|
4,2 x 10-3 |
|
t(%) |
|
4,2 |
|
Qreq |
|
1,8 x 10-4 |
c) Comparer la
valeur expérimentale Qr,eq avec la valeur de la constante KA
du couple HCOOH, HCOO-.
Q4
On réalise la même
étude, en utilisant une solution S1 d’acide formique de
concentration C1 = 0,10 mol.L-1. Les résultats obtenus
sont indiqués dans le tableau ci-dessus. En déduire l’influence de la
concentration de la solution sur :
a)
le taux d’avancement
de la réaction
b)
le quotient de
réaction dans l’état d’équilibre.