Chapitre 6 : réaction acidobasique, titrage
Dosage d'un vinaigre (Ministère)
(D'après
Guadeloupe, Guyane, Martinique Juin 2001)
On se propose
de doser par pH-mètrie un vinaigre afin d'en déterminer la concentration
molaire volumique en acide éthanoïque. Pour cela, on prépare V = 100 mL d'une
solution diluée 10 fois du vinaigre.
Puis
on prélève un volume V1 = 10 mL de la solution diluée que l'on
verse dans un bêcher, auquel on ajoute suffisamment d'eau distillée pour
immerger correctement la cellule du pH-mètre. On réalise le dosage avec une
solution d'hydroxyde de sodium de concentration molaire volumique c2 = 1,0
× 10-1 mol.L.-1.Le
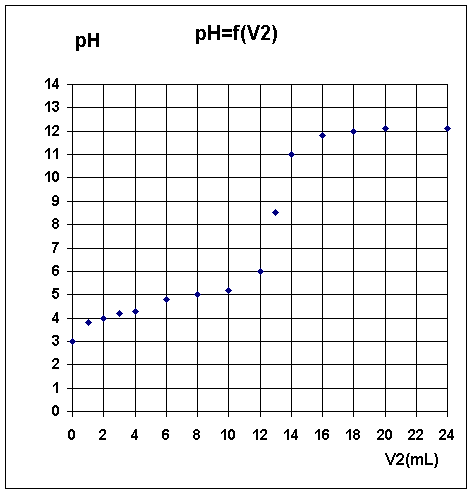
pH est relevé en fonction du volume V2 de solution d'hydroxyde de
sodium et on obtient la courbe pH = f(V2) donnée en annexe. Toutes les
solutions considérées sont prises à 25°C.
Donnée
: pka du couple CH3COOH / CH3COO-
à 25 °C : pka = 4,8 et pKe = 14.
Q1
a) Ecrire l'équation chimique
associée à la transformation du système étudié.
b) Exprimer le quotient de réaction Qr de cette réaction.
c) Quelle valeur particulière ce quotient de réaction
prend-il dans l'état
d'équilibre du système ? Calculer
cette valeur.
d) Cette valeur dépend-elle
de la composition initiale du système ?Quelle hypothèse faut-il faire
sur la nature dela transformation chimique
pour que la
réaction
puisse servir de support au dosage ?
Q2
a) Déterminer graphiquement les coordonnées du point d'équivalence acido-basique E, en utilisant
le graphe en annexe. Donner la méthode utilisée.
b) Quelles sont les
espèces chimiques majoritaires à
l'équivalence ?
Q3
a) On note n1
la quantité de matière
de réactiftitr é initialement apporté dans le
bêcher et n2éq la quantité de
matière de réactif
titrant versé à
l'équivalence. Établir la relation liant n1 et n2éq.
b) En déduire la concentration c1 en acide éthanoïque
apporté dans la solution diluée.
c) Calculer la
concentration c en acide
éthanoïque du vinaigre.
Q4
a) On se place
dans la situation
où on a versé un volume
d'hydroxyde de sodium
représentant la moitié du volume
versé à l'équivalence. Quelles
sont les quantités
d'hydroxyde de sodium et d'acide
éthanoïque introduites alors ?
b) A l'aide d'un tableau descriptif de l'évolutiondu système, déterminer la
quantité d'ion éthanoate alors
formé, ainsi que
la quantité d'acideéthanoïque restant dans le milieu
réactionnel.
c) En déduire la valeur du pH en ce
point
d) Comparer la valeur du pH ainsi trouvée avec la valeur du
pH lue sur la courbe
de dosage. Commenter