Chapitre 6 : créer et
reproduire des espèces chimiques
ÉTUDE DE mÉdicaments à base
d'ASPIRINE (Nouvelle Calédonie Novembre
2007)
L'acide acétylsalicylique,
ou aspirine, est le médicament le plus vendu dans le monde.
Cependant, la prise
d'aspirine n'est pas sans danger, elle peut provoquer des ulcères à l'estomac
ou
être à l'origine de saignements. C'est afin de limiter ces risques que ce
médicament se présente sous différentes formulations. On se propose dans cet
exercice d'en étudier deux : l'aspirine simple et
l'aspirine pH8.
Données:
Formule de l'acide acétylsalicylique
:
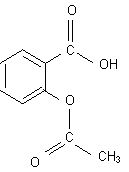 L'acide
acétylsalicylique sera noté AH et l'ion acétylsalicylate
A –.
L'acide
acétylsalicylique sera noté AH et l'ion acétylsalicylate
A –.
La forme AH est liposoluble(soluble
dans les lipides) tandis que la forme A–
est hydrosoluble.
La muqueuse de l'estomac
(muqueuse gastrique) présente des lipides au niveau de ses tissus.
Masse molaire : M(acide
acétylsalicylique ) = 180 g.mol –1.pKa du couple acide
acétylsalicylique / ion acétylsalicylate (AH / A–) : 3,5 à la température de
l'étude expérimentale.
pH estomac = 2 ;
pHintestin = 8.D'après la notice de l'aspirine
simple :
COMPOSITION :
Acide acétylsalicylique
..................…...... 500 mg
Excipients : Amidon de maïs, poudre de
cellulose granulée
FORME PHARMACEUTIQUE : Comprimés
CLASSE PHARMACOTHÉRAPEUTIQUE : Antalgique
périphérique, antipyrétique
MODE ET VOIE D'ADMINISTRATION :
Voie orale. Boire immédiatement après
dispersion complète des comprimés dans un grand verre
d'eau, de préférence au moment des repas.
D'après la notice de
l'aspirine pH8 :
COMPOSITION QUALITATIVE :
Acide acétylsalicylique ……………………...500 mg
Excipients : Amidon de riz, acétophtalate cellulose, phtalate
d'éthyle
FORME PHARMACEUTIQUE : Comprimé gastro-résistant
CLASSE PHARMACOTHÉRAPEUTIQUE :
Antalgique périphérique, antipyrétique,
anti-inflammatoire à dose élevée, antiagrégant plaquettaire
MODE ET VOIE D'ADMINISTRATION :
Voie orale. Les comprimés sont à avaler tels
quels avec une boisson (par exemple eau, lait, jus de
fruits).
1. Questions préliminaires
1.1. 1.1. Recopier
la formule de l'aspirine et préciser après l’avoir encadrée, la fonction acide
carboxylique.
1.2. Tracer
le diagramme de prédominance des espèces chimiques du couple AH /A –
.
Sous quelle forme, AH ou A–,
l'organisme assimile-t-il l'aspirine dans l'estomac et dans l'intestin ?
Calculer le
rapport des concentrations ![]() à pH = 7. Quelle est l’espèce prédominante à ce pH ?
à pH = 7. Quelle est l’espèce prédominante à ce pH ?
2. L'aspirine simple
2.1.
Pourquoi l'aspirine simple
est-elle absorbée par la muqueuse gastrique ?
2.2.
Justifier le mode
d'administration de cette formulation d'aspirine décrit dans le texte.
2.3. Afin de vérifier
l'indication « 500 mg » de la notice, on saponifie l'aspirine par un excès de
soude
et on dose cet excès par une solution d'acide chlorhydrique.
Le protocole opératoire est le suivant :
Introduire dans un ballon un comprimé d'aspirine
simple, 10 mL d'eau distillée, 10,0 mL de solution de
soude de concentration molaire cB =
1,0 mol.L–1 et quelques grains de pierre ponce.
Chauffer le mélange à reflux pendant une
vingtaine de minutes.
Verser le contenu refroidi du ballon dans
une fiole jaugée de 100,0 mL, récupérer l'eau de
rinçage et compléter le niveau au trait de jauge avec de l'eau distillée.Doser alors 10,0 mL de
cette solution par une solution d'acide chlorhydrique de concentration molaire cA = 5,0 ´ 10 –2 mol.L–1 en présence de phénolphtaléine. Expérimentalement,
le volume équivalent d'acide versé vaut : VAE = 8,4 mL.
La réaction de saponification de l’aspirine est
modélisée par l'équation chimique suivante :
(1) AH + 2
HO – = C7H5O2- + CH3CO2 – + H2O
L'indicateur coloré choisi permet de ne doser que la
base HO – présente dans le milieu.
L'équation support du dosage s'écrit :
(2) H3O+ + HO – = 2 H2O
2.3.1.
Calculer la quantité de
matière ni (HO – ) d'ions hydroxyde introduits dans le
ballon.
2.3.2.
Déduire du volume équivalent
versé, la quantité de matière n d'ions hydroxyde en
excès présente dans le prélèvement de
10,0 mL puis la quantité de matière n’ d'ions hydroxyde en
excès présente dans les 100,0 mL de départ.
2.3.3.
Dessiner un tableau
d’avancement de l'équation (1) en utilisant uniquement des expressions
littérales. On utilisera les abréviations suivantes :
aspirine : AH. La quantité de matière d’aspirine
est notée n(asp).
2.3.4 Déterminer la quantité d'aspirine n(asp) présente dans le ballon.
2.3.5 En déduire la masse m d'aspirine
contenue dans le comprimé.
Calculer l'écart relatif: ![]()
Le résultat confirme-t-il l'indication
« 500 mg » de la notice ?
3.
L'aspirine
pH8
Expériences :
A – On dispose de deux
béchers contenant respectivement 50 mL de solution
d'acide chlorhydrique et
50 mL de solution de soude. Les deux solutions ont la
même concentration molaire : 0,1 moL.L –1.
On ajoute dans chacun d'eux
un comprimé d'aspirine pH8 et on agite.
Après quelques minutes, on constate que le comprimé
s'est dissous dans le bécher contenant la
solution de soude alors que le comprimé ajouté dans la solution d'acide reste
intact.
B - Dans un bécher contenant 50 mL
d'eau distillée additionnée de quelques gouttes de bleu de bromothymol,
on introduit un comprimé d'aspirine pH8. Le bleu de bromothymol
apparaît alors bleu
(sa couleur en milieu basique). On écrase ensuite le comprimé, détruisant ainsi
son enrobage, le bleu
de bromothymol vire alors au jaune (sa couleur en
milieu acide).
3.1.
Interpréter l'expérience A et justifier l'indication de la
notice « comprimé gastro-résistant ».
3.2.
On qualifie l'aspirine pH8 d'aspirine « retard », pourquoi ?
3.3.
Interpréter l'expérience B pour expliquer pourquoi, d'après
la notice, les comprimés doivent être avalés « tels quels » (c'est à dire sans
les croquer).