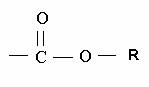Chapitre 10 :
estérification hydrolyse
|
I) Les
esters 1) Définition Un ester est un
composé organique qui possède le groupe caractéristique : La formule générale
des esters s'écrit : 2) Nomenclature La première partie
désigne la chaîne carbonée contenant le carbone fonctionnel : on remplace la
terminaison oîque de l'acide carboxylique correspondant par "oate".
La seconde partie désigne la chaîne liée à l'atome d'oxygène: elle est nommée
comme un radical alkyle. II)
Equilibre d'estérification hydrolyse 1) Caractéristiques de la
réaction d'estérification On réalise un mélange
d'acide carboxylique et d'alcool. La réaction produit un ester et de l'eau
suivant l'équation bilan suivante :
R-CO2H + R'-OH = R-CO2-R' + H2O La réaction
d'estérification est lente, limitée, athermique. |
2) Caractéristiques de la réaction d'hydrolyse d'un ester La réaction inverse de
la réaction d'estérification est appelée réaction d'hydrolyse. R-CO2-R'+H2O
= R-CO2H+R'-OH L' hydrolyse d'un
ester est une réaction lente, limitée, athermique.
Son taux d'avancement final est inférieur à un. 3) L'équilibre
d'estérification hydrolyse La réaction
d'estérification est la réaction inverse de l'hydrolyse de l'ester. Ces deux
réactions se limitent mutuellement. La constante
d'équilibre K de la réaction d'estérification est :
La constante
d'équilibre K' de la réaction d'hydrolyse de l'ester est l'inverse de celle
de l'estérification :
L'eau est un des produits de la réaction et non plus le solvant : il
faut faire intervenir sa concentration dans la constante d'équilibre. Pour
aller à la page 2 clique ici. |